

- 首 页
- 关于我们
- 环境丰容
- 笼器具
- 实验器械
- 仪器设备
- 病理产品
- 试剂耗材
- 实验服务
- 科技学苑


环境丰富对兔应激的影响
刘鹍 谢晓婕 兰青 卫澜欣 易兵 赖润秋 熊敏 刘斌
(成都华西海圻医药科技有限公司,成都 610041)
摘要:目的 为了探索环境丰富对动物福利生活和应激水平的影响,摸索不同饲养环境丰富方式(食物、环境、人文丰富)对动物健康生长的影响。方法 实验将24 只新西兰白兔,雌雄各半,随机分为6 组,每组4 只,即阴性对照组(A组,单一玩具,一周更换一次)、对照组(B组,无任何环境丰富)和丰容组(分为4组,每组玩具更换频率依次为3、6、9和12 d,分别为C、D、E和F组)。实验周期为3周,研究了环境丰富频率对新西兰白兔行为、血液学指标、尿液中皮质酮和促肾上腺皮质激素、脑组织中抗凋亡蛋白(Bcl-2)、Caspase-3以及脑组织中相关mRNA基因表达情况的影响。结果 动物行为学观察显示,与B组相比,F组差异有统计学意义(P<0.05),E组差异有统计学意义(P<0.01);动物在3周的时间内,血液学指标和尿液中激素含量均未见显著性差异;动物脑组织中相关基因表达情况显示,和B组相比,环境丰富C、D和F组中脑源性嗜神经因子(BDNF)基因表达量差异有统计学意义(P<0.05),与B组相比,D组中糖皮质激素受体(GR)基因表达量差异有统计学意义(P<0.05),与A和B组相比,C和F组中TH基因表达量差异有统计学意义(P<0.05),与B和C组相比,D和F组中酪氨酸羟化酶(TH)基因表达量差异有统计学意义(P<0.05);除此之外,促黑素细胞皮质素原(POMC)和色氨酸羟化酶(TPH)基因表达量在各组中未见差异;动物脑组织中抗凋亡蛋白(Bcl-2)的表达结果显示,与B组相比,C、D、E、F组脑组织中Bcl-2蛋白的表达量均呈增加趋势。Caspase-3蛋白的表达结果显示,与B组相比,A、C、D、E组脑组织中Caspase-3蛋白的表达量均呈减少趋势。结论 增加环境丰富以及食物丰富后,一定程度上能改善兔抗应激能力,并不会对兔血液学相关指标造成影响;当对实验兔进行环境丰富时,应该避免对兔环境频繁地改变,在保持玩具清洁的前提下,玩具类型更换频率以6d一次最佳,兔脑神经更富活力,对于痛苦和恐惧的调节能力更强,更具安全感;当玩具类型使用频率过高(3d更换一次),可能会使实验兔的应激加剧。
关键词: 环境丰富度;新西兰白兔;应激;动物福利
环境丰富(environmental enrichment)又称环境丰富度,其目的是为了让动物能享有表达天性自由,可以丰富食物类型、笼内玩具、饲养方式、提供音乐和视频等手段来实现,不同种属的动物,根据动物生物特性存在差异,其使用的环境丰富产品也有所不同。
适当的环境丰富可以降低动物血液中应激激素的浓度,但高频更换新奇的玩具可能会对动物造成新的应激[1]。亦有研究表明,环境丰富能改善噪音刺激所引起的小鼠焦虑反应[2]。除此之外,环境丰富的执行,在提高动物福利的同时也能有助于提高动物实验结果的准确性[3]。由于实验动物的特殊性,存在因实验过程导致动物表现出行为异常,如刻板症和自残等。相关研究报道,环境丰富对降低长期单笼饲养食蟹猴异常行为也有积极的显著影响[4],环境所带来的丰富且适宜的刺激,可以改善脑组织的可塑性并提升动物的学习能力,能有效的抵御压力带来的多种负面影响,从而能调节机体的激素稳态,帮助控制动物情绪变化,提高学习和记忆能力等。与此同时,过强的应激反应可造成动物生理以及免疫指标发生异常[5]。动物在应激条件下,下丘脑—垂体—肾上腺皮质(HPA)轴被激活,最终促进皮质酮合成分泌的增加[6]。所以动物的应激程度可以通过行为学或皮质醇的水平来监测。另外,机体长时间处于应激状态时,血中皮质酮浓度会呈现下降趋势,这可能是由于机体出现负反馈调节的结果[7]。
虽然上述各项指标相关的研究层出不穷,但将其用于评价环境丰富对实验兔的福利水平相关的研究甚少,为了探究环境丰富对动物福利的影响,本文通过应激生物学实验评价实验动物的福利状况,以期探索不同饲养环境丰富方式(食物、环境、人文丰富)对兔的抗应激能力的影响。
1 材料和方法
1.1 材料
1.1.1 实验动物和动物饲养:动物选取普通级新西兰白兔24只,雌雄各半,年龄为5~6月龄,体质量2.5~5.0kg,来源于邳州市东方养殖有限公司,生产许可证号为SCXK(苏)2022-0004;本机构实验动物使用许可证为SYXK(川)2023-0123。
本机构通过AAALAC国际(AAALAC International)认可。本实验在活体动物饲养阶段,在成都华西海圻医药科技有限公司一栋中小区1219实验室进行;本实验涉及的与动物实验相关的内容和程序都遵从国家标准GB/T 35892《实验动物福利伦理审查指南》和本机构实验动物管理和使用委员会(Institutional Animal Care and Use Committee,IACUC)的相关规定,同时遵从实验动物饲养管理和使用指南第八版。
本实验通过了本单位实验动物福利伦理委员会的审批,伦理审批号为IACUC-S2023010。
1.1.2 试剂与仪器:无水乙醇(四川西陇科学有限公司)Western及IP细胞裂解液(上海碧云天生物技术有限公司);磷酸酶抑制剂(Biosharp公司);BCA蛋白浓度测定试剂盒(上海碧云天生物技术有限公司);SDS-PAGE蛋白上样缓冲液(Biosharp公司);预染蛋白Marker(Yeasen公司);Immobilon-PSQ PVDF膜(Sigmaaldrich公司);NaCl(天津市致远化学试剂有限公司);脱脂奶粉(Servicebio公司);Tubulinβ(Affbiotech公司);Bcl-2(Abclonal公司)。
实时荧光定量(RT-PCR)仪(美国ThermoFisher仪器有限公司);旋涡混合器(江苏康健医疗用品有限公司);电子天平(美国康州HZ电子科技有限公司);手提式不锈钢压力蒸汽灭菌器(上海申安医疗器械厂);台式高速冷冻离心机(湘仪集团);荧光图像分析系统(Tanon公司)。
1.2 方法
1.2.1 动物分组和环境丰富:实验将24 只新西兰白兔,雌雄各半,随机分为6 组,每组4 只,即阴性对照组(A组,单一玩具,一周更换一次)、对照组(B组,无任何环境丰富)和丰容组(分为4 组),每组玩具更换频率依次为3、6、9和12 d更换一次,分别为C、D、E和F组。每组动物经口灌胃0.9%氯化钠溶液,每两天1次。
另外,本研究中使用经口灌胃0.9%氯化钠溶液的方式,各组所有动物按每2 d一次的频率给予操作刺激。本研究中选取新西兰白兔进行环境丰富,具体环境丰富如笼内玩具丰富、食物丰富、人文友善的交流等,频率为每3、6、9、12 d换一次,动物数量共24 只。实验兔笼内玩具,可使用如塑料铃球、塑料啃材、木块、木棍等,按照丰容频率进行更换;实验兔食物丰富,可使用提摩西干草、新鲜蔬菜、大蒜、苜蓿草等每天饲喂。将动物分为对照组、阴性对照组和环境丰富组,具体环境丰富情况见图1。

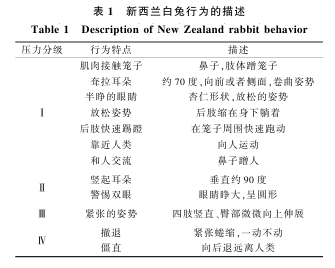
1.2.2 动物行为学观察:每日定时,根据表2中动物行为特点观察新西兰白兔行为变化,记录动物压力等级,详细情况如表1所示。
1.2.3 标本采集与取材:血液采集,采样检测前动物禁食至少12 h,不禁水,采样位置为动物耳中动脉。测定指标包括白细胞数(WBC)、红细胞数(RBC)、血红蛋白(HGB)、红细胞压积(HCT);血生化检测指标包括:谷丙氨酸酶(ALT)、总胆红素(TBIL)、尿素(UREAL)和甘油三酯(TG)。
脑组织采集:实验结束时,使用3%的戊巴比妥钠,按照30mg/kg的剂量以静脉注射的方式麻醉动物,开胸放血后,揭开动物颅骨,摘取动物脑组织,以-80℃冷冻保存。尿液采集,底盘收集。
1.2.4 双抗夹心ELISA检测尿液中应激激素ACTH和CORT浓度测定:尿液中应激激素的测定采用双抗夹心酶联免疫吸附实验(ELISA),将目标抗体包被于96孔微孔板中,制成固相载体,向微孔中分别加入标准品或者样本,其中的目标连接于固相载体上的抗体结合,然后加入辣根过氧化物酶标记的抗体,将未结合的抗体洗净后再次加入TMB底物显色。TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的目标呈正相关。用酶标仪在450nm波长下测定吸光度(A值),计算样品浓度。
1.2.5 荧光定量PCR检测脑组织中GR、POMC、BDNF、TH和TPH相关mRNA基因相对表达量:引物设计合成,从美国国家生物技术信息中心(NCBI)数据库中搜索基因全序列,使用PrimerPremier引物设计软件设计筛选各基因特异性引物。所有引物均交由上海生工生物工程技术服务有限公司设计合成,并以ULTRAPAGE纯化(表2)。提取Hirt DNA后,以DNA作为模板,进行实时荧光定量PCR检测,结果采用2-△△Ct计算方法表示。

1.2.6 Western blot检测脑组织Caspase-3/Bcl-2蛋白的表达:样品蛋白制备完成后,计算各组蛋白浓度使其保持一致,变性完成后-80℃保存。待到SDSPAGE凝胶凝聚后,通过转膜、封闭、孵育一抗、孵育二抗后,准备一个干净干燥的玻璃皿,将ECL发光液的A、B两种试剂在玻璃皿中等体积混合后,放入避光环境。把PVDF膜在避光环境下完全浸没在含有ECL混合液的培养皿中,之后取出膜放置于曝光板上,将曝光板放入Tanon 荧光图像分析系统的暗室中,根据信号的强弱适当调整曝光时间,曝光。图像分析:用Tanon 荧光图像分析系统软件V2.0对条带进行曝光,结果以Gel-Pro analyzer4软件扫描曝光结果,并以目的蛋白积分吸光度(IA)表示。
1.3 统计学分析
所有定量指标均分性别进行统计分析。首先采用Levene检验评估方差齐性: 方差齐性时(P>0.05),采用单因素方差分析(ANOVA)进行组间比较。若ANOVA结果显示差异有统计学意义(P≤0.05),则进一步使用最小显著差异法(LSD法)进行两两比较;若P>0.05则终止分析。方差不齐时(P≤0.05),采用Kruskal-Wallis H秩和检验(K-W法)进行非参数检验。若K-W检验结果显示差异有统计学意义(P≤0.05),则采用Mann-Whitney U检验(M-W法)进行两两比较;若P>0.05则终止分析。所有检验均为双侧检验,显著性水平设为α=0.05。数据分析使用Stata/IC 15.0 for Windows完成,图表绘制采用GraphPad Prism 8.1。
2 结果
2.1 动物行为学观察压力水平评估
在为期21 d的实验中,每天定时16:00—17:00观察动物行为学特点,对动物压力水平进行评级,统计数据如图2所示,其中阴性对照组与对照组比较,差异无统计学意义,与A和B组相比,E组和F组差异有统计学意义(P<0.01,P<0.05)。

2. 2 环境丰富措施对新西兰白兔部分血液生化指标的影响
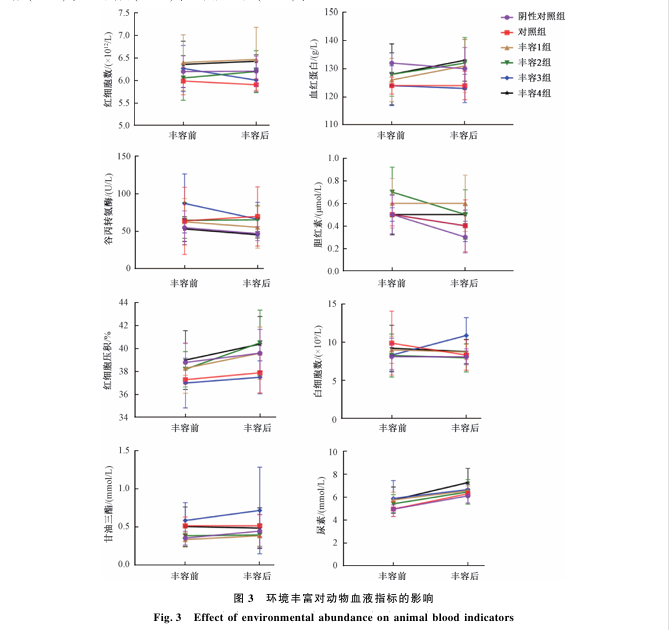
本研究监测了环境丰富第1天以及第21天时,动物的血液生化指标包括白细胞数(WBC)、红细胞数(RBC)、血红蛋白(HGB)、红细胞压积(HCT)、谷丙氨酸酶(ALT)、总胆红素(TBIL)、尿素(UREAL)和甘油三酯(TG)的含量;研究结果发现,如图3 所示,经过环境丰富前后,动物血液生化指标均不存在差异。
2. 3 环境丰富措施对新西兰白兔应激激素的影响
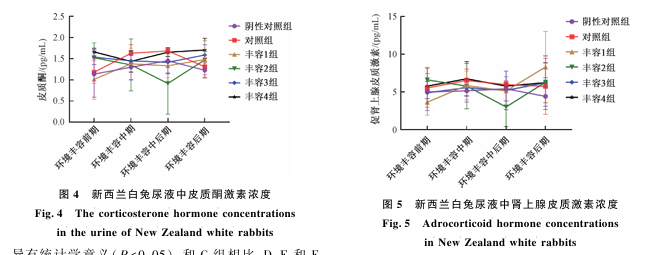
如图4,5 所示,环境丰富后,采集了动物尿液进行应激激素的检测,检测结果显示:各组之间均未见差异性,短期的环境丰富可能对新西兰白兔尿液中应激激素影响较小。
2. 4 环境丰富措施对新西兰白兔脑组织中 GR、POMC、BDNF、TH 和 TPH 相关 mRNA 基因表达的影响
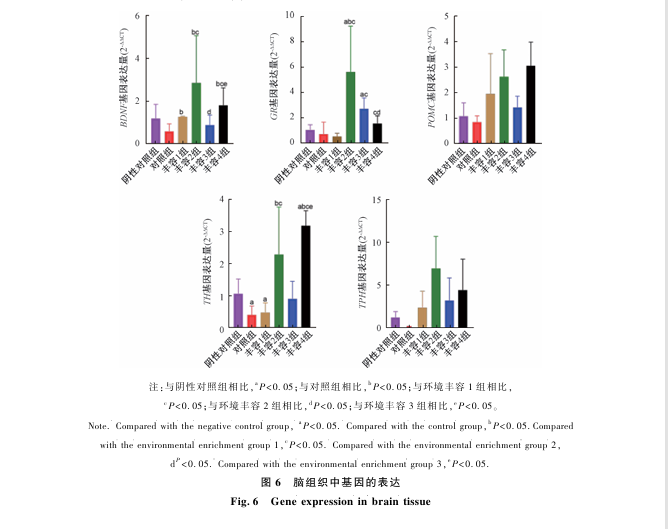
如图6所示,和B组相比,C、D和F组中BDNF基因表达量差异有统计学意义(P<0.05),和C组相比,D和F组BDNF基因表达量差异有统计学意义(P<0. 05),和 D组相比,E组中BDNF基因表达量差异有统计学意义(P<0.05),和E组相比,F组中BDNF基因表达量差异显著(P<0.05);和B组相比,D和E组中GR基因表达量差异有统计学意义(P<0. 05),和B组相比,D组中GR基因表达量差异有统计学意义(P<0.05),和 C组相比,D、E和F组中GR基因表达量差异有统计学意义(P<0.05),和D组相比,F组中GR基因表达量差异有统计学意义(P<0.05);和A组相比,B、C和F组中TH基因表达量差异有统计学意义(P<0.05),与B组和C组相比,D和F组中TH基因表达量差异有统计学意义(P<0.05),和E 组相比,F组中TH基因表达量差异有统计学意义(P<0.05)。除此之外,POMC和TPH 基因表达量在各组中未见差异。
2.5 环境丰富措施对新西兰白兔脑组织中Caspase-3/Bcl-2表达的影响
如图7,8所示,和对照组相比,阴性对照组和环境丰富各组脑组织中Bcl-2蛋白的表达量均呈上升趋势,而和B组相比,A、C、D和E组中Caspase-3蛋白的表达量减少。

3 讨论
本文通过对实验兔进行环境丰富,研究丰容前后,对其生物学相关指标以及凋亡相关蛋白表达情况的影响。研究结果发现,环境丰富和每两天一次的灌胃操作并不会对实验兔的血液学相关指标(WBC、RBC、HGB、HCT、ALT、TBIL、UREAL和TG)造成影响。与此同时,在实验期间对动物的行为学特点进行了压力分级,分析结果发现,在对实验动物增加食物丰富和环境丰富的同时,每6、9或12 d更换一次玩具,对动物行为应激较小,频繁地更换玩具(如3 d更换一次)可能会掩盖环境丰富对兔抗应激的作用。
本文还研究了环境丰富对脑组织细胞凋亡的影响,凋亡存在于哺乳动物生长发育的全阶段,其形态学上表现为细胞核以及胞质的浓聚,凋亡小体的出现。其中Bal-2基因是Bcl-2家族中的抗凋亡基因,具有抗凋亡的作用,在凋亡线粒体通路上起到关键的作用。相关研究表明,动物在应激状况下会发生行为学以及神经系统的改变,极度或慢性的应激会引起大脑星形胶质细胞发生凋亡,其影响包括学习和认知障碍以及与应激相关的神经精神紊乱,如焦虑、抑郁、创伤后应激障碍等 [8-10]。研究结果发现,和对照组相比,在环境丰富后,阴性对照组和环境丰富各组脑组织中Bcl-2蛋白的表达量均呈上升趋势,而和B组相比,A、C、D和E组中Caspase-3蛋白的表达量减少,这也在一定程度上说明了适当的环境丰富能影响神经系统的改变,缓解动物的焦虑。
与此同时,本实验还通过研究脑神经相关基因的表达,评估了环境丰富对动物福利的影响,其中包括BDNF、TH、TPH、POMC、GR,其中BDNF是哺乳动物大脑中分布最广、数量最丰富的神经生长因子家族成员之一[11],与许多神经系统疾病的发生和发展密切相关[12]。BDNF是抗抑郁药与卒中后恢复之间复杂相互作用的关键因子[13]。除此之外,相关研究还表明,BDNF可以预防缺血性脑损伤,并减少葡萄糖剥夺后的神经元凋亡[14]。通过实验发现,和未进行环境丰富的动物相比,环境丰富的实验组中,BDNF基因表达量呈上升趋势,而每3、6、12 d更换一次动物玩具,动物脑组织中BDNF表达量显著增加(P<0.05),在予以环境和食物丰富的情况下,每6 d更换一次玩具的环境丰富频率下,动物脑神经更富活力,动物对于痛苦和恐惧的调节能力更强,更具安全感。
另外,TH是儿茶酚胺合成的限速酶。儿茶酚胺多巴胺、肾上腺素和去甲肾上腺素是该途径的产物,这些物质作为激素和神经递质在中枢和周围神经系统中起到关键的作用[15]。并且相关研究表明,儿茶酚单胺在许多大脑功能中发挥作用,如注意力、记忆、认知和情绪[16]。实验结果显示,与A组和B组相比,每6、12 d更换一次动物玩具,动物脑组织中TH基因表达量显著上调,该频率让动物对环境维持更高的新鲜感。
我们还考察了兔大脑组织中TPH和POMC的基因表达量的变化,其中TPH可以使色氨酸的C5羟基化,其过程是抑郁症发病的重要机制之一,色氨酸羟化酶若受到抑制,可能会引发抑郁症[17-19]。而POMC基因的表达情况,POMC的衍生物黑皮质素是β内啡肽的前体,研究表明,β内啡肽在控制应激激素分泌中起着“负调节作用”[20-21]。本研究结果发现,环境丰富并不会使TPH和POMC的基因表达量发生明显的改变。
与此同时,研究还发现,各组中GR基因的表达量也存在显著差异,其中D、E和F组之间较其他各组动物GR表达量显著增高,其表达量反应动物急性应激水平,造成该情况的原因尚不明确,需要在后续实验中进一步研究。
综上所述,增加环境丰富以及食物丰富后,一定程度上能改善兔抗应激能力,并不会对兔血液学相关指标造成影响;当对实验兔进行环境丰富时,应该避免对兔环境频繁地改变,在保持玩具清洁的前提下,玩具类型更换频率以6 d一次最佳,兔脑神经更富活力,对于痛苦和恐惧的调节能力更强,更具安全感;当玩具类型使用频率过高(3d更换一次),可能会使实验兔的应激加剧。
参 考 文 献
[1] 刘帅,宋佳阳,吕赛,等.环境丰富对SD大鼠行为和肾上腺皮质激素的影响研究[J].中国比较医学杂志,2020,30(12):92-97.
[2] 陈枉枉,肖春兰,王艳,等.丰容环境对噪声引起的小鼠焦虑改善作用及机制研究[J].扬州大学学报(农业与生命科学版),2020,41(6):102-106.
[3] 高建峰,滕利,郭铭,等.环境丰富对长期单笼圈养食蟹猴行为的影响[J].四川动物,2016,35(2):243-248.
[4] 国家质检总局.实验动物 福利伦理审查指南:GB/T 35892—2018[S].2018.
[5] 张学英,艾洪滨,孙西寨.应激性对动物免疫功能影响的研究进展[J].生物学通报,2003,38(10):9-11.
[6] 江健康,付常喜.水环境对大鼠下丘脑-垂体-肾上腺皮质轴激素的影响[J].内江科技,2009,30(3):27-29.
[7] 刘雁峰,王天芳,杨维益,等.复合应激因素致大鼠促肾上腺皮质激素和皮质酮含量变化的研究[J].中国医药学报,2000,15(1):72-74.
[8] 董丽儒,连俊波,霍双杰,等.慢性束缚应激对大鼠杏仁核细胞凋亡的影响[J].法医学杂志,2022,38(4):459-467.
[9] LINDQVIST D,DHABHAR F S, JAMES S J, et al. Oxidative stress, inflammation and treatment response in major depression[J]. Psychoneuroendocrinology,2017(76):197-205.
[10] GHAFFARI-NASAB A, JAVANI G, YOUSEFI H, et al.Prolonged stress-induced depression-like behaviors in aged rats are mediated by endoplasmic reticulum stress and apoptosis in the hippocampus[J]. Neurosci Res,2024(198):39-46.
[11] BEGNI V, RIVA M A, CATTANEO A. Cellular and molecular mechanisms of the brain-derived neurotrophic factor in physiological and pathological conditions[J]. Clin Sci (Lond), 2017(131):123.
[12] LEE J, JIFFAR T, KUPFERMAN M E. A novel role for BDNFTrkB in the regulation of chemotherapy resistance in head and neck squamous cell carcinoma [J]. PLoS One, 2012(7):e30246.
[13] MORAIS V, TOURINO M, ALMEIDA A, et al. A single session of moderate intensity walking increases brain-derived neurotrophic factor (BDNF) in the chronic post-stroke patients[J]. Top Stroke Rehabil, 2018(25):118.
[14] LIANG J, YUE Y, JIANG H, et al. Genetic variations in the p11/ tPA/BDNF pathway are associated with post stroke depression[J]. J Affect Disord, 2018(226):313-325.
[15] DAUBNER S C, LE T, WANG S. Tyrosine hydroxylase and regulation of dopamine synthesis[J]. Arch Biochem Biophys, 2011(508):1-12.
[16] WILLEMSEN M A,VERBEEK M M, KAMSTEEG E J, et al. Tyrosine hydroxylase deficiency: a treatable disorder of brain catecholamine biosynthesis[J]. Brain, 2010(133):1810-1822.
[17] JACOBSEN J P R, SIESSEV W B, SACHS B D,et al. Deficient serotonin neurotransmission and depression-like serotonin biomarker alterations in tryptophan hydroxylase 2 (Tph2) loss-of function mice[J]. Mol Psychiatry, 2012,17(7):694-704.
[18] WALTHER D J, PETER J U, BASHAMMAKH S,et al. Synthesis of serotonin by a second tryptaphan hydroxylase isoform[J]. Science, 2003,299(5603):76.
[19] WILLNER P, SCHEEL-KREGER J, BELZUNG C,et al. The neurobiology of depression and antidepressant action [J]. Neurosci Biobehav Rev, 2013(37):2331.
[20] GONCALVES, G H M, LI W J, GARCIA A V C G,et al. Hypothalamic agouti-related peptide neurons and the central melanocortin system are crucial mediators of leptin’epantidiabetic actions[J]. Cell Rep, 2014,7(4):1093-1103.
[21] APONTE Y,ATASOY D, STERNSON S N, et al. AGRP neurons are sufficient to orchestrate feeding behavior rapidly and without training[J]. Nat Neurosci,2011, 14(3):351-355.

400 - 102 - 1174


咨询热线

莱
艾
特
商
城
扫
一
扫
关
注

京ICP备14028330号-1 京公网安备 11010802039490号
Copyright © 2015 All Rights Reserved www.bjlat.com 设计维护:北京莱艾特科技发展有限公司
郑重声明:引用他人的信息,本网站均已经列明出处。
转载的目的在于学术交流与讨论,若有任何侵犯您的权益之处,请与我们联系删除相关内容。
地址:北京市海淀区天秀路10号中国农大国际创业园3号楼2层2002 邮箱:info@bjlat.com 电话:010-62969989;13661392264
































































